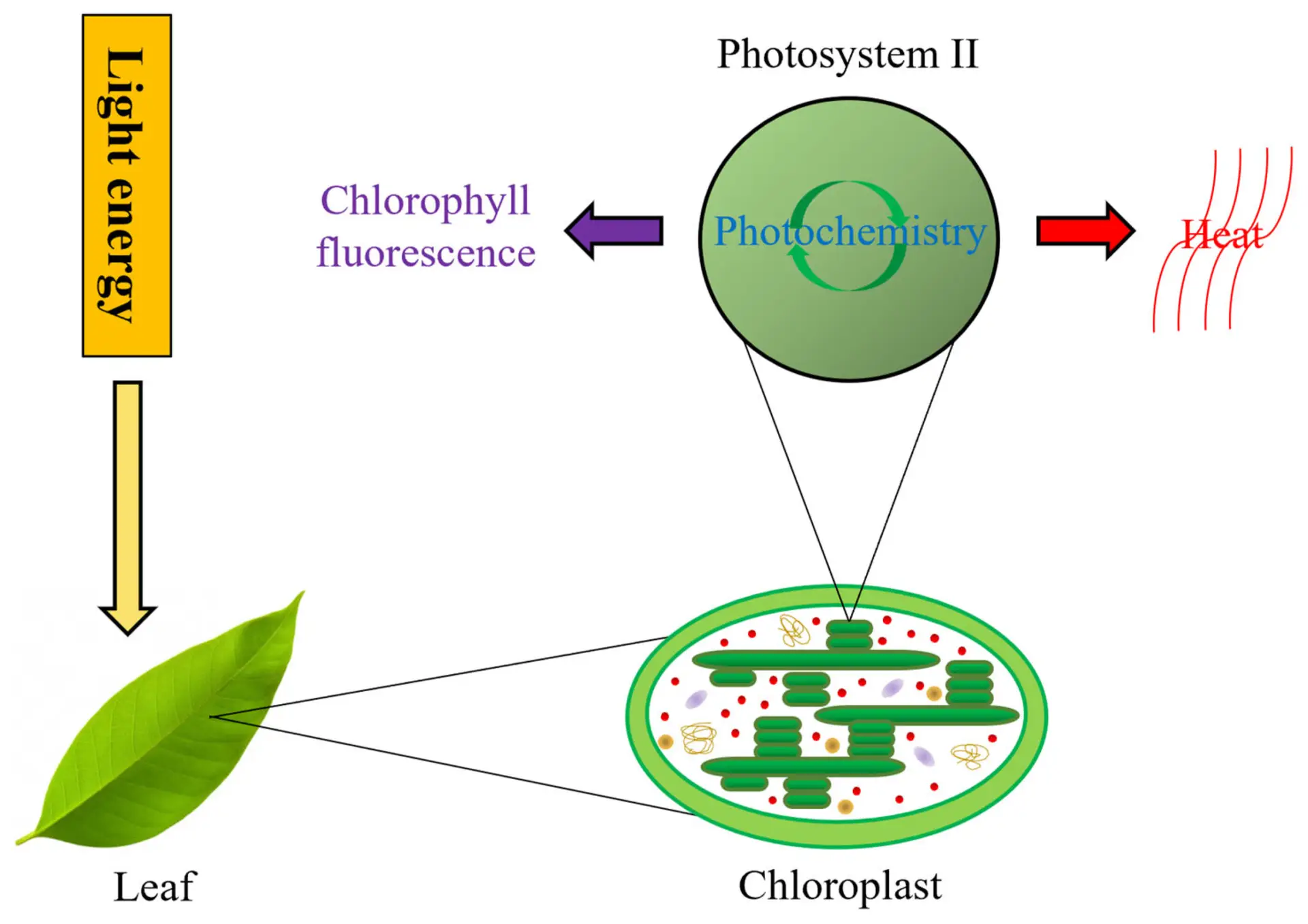
在叶绿素荧光成像测量中,光化光(Actinic Light, AL)强度的设置是实验成功的关键之一,它没有唯一的“标准值”,但有一个需要根据实验目的来确定的“适宜范围”。
一、光化光强度的一般设置范围
通常,光化光强度设置在 100 到 1000 µmol photons m⁻² s⁻¹ 之间是一个常见的范围。具体设置为多少,主要取决于:
1、研究对象的生长光强(最关键因素):这是最重要的参考依据。为了真实反映植物在自然状态下的生理情况,光化光强度应模拟其原生环境的光强。
- 阴生植物(如蕨类、某些观叶植物):通常设置在 50 – 200 µmol m⁻² s⁻¹。
- 阳生植物(如小麦、玉米、拟南芥):通常设置在 300 – 800 µmol m⁻² s⁻¹,甚至更高,以模拟全光照条件。
- 藻类或水生植物:设置可能更低,例如 20 – 100 µmol m⁻² s⁻¹。
2、实验目的:
- 光合诱导曲线:通常从一个较低的光强开始,然后逐步增加光化光强度,以观察植物对不同光强的适应过程。
- 光响应曲线:需要设置一系列梯度光强(如 0, 50, 100, 200, 500, 800, 1000, 1500…),来绘制参数(如Y(II), NPQ, ETR)随光强变化的曲线。
- 胁迫生理研究:如果要研究强光胁迫,可能会设置远高于生长光强的光化光(如 1500-2000 µmol m⁻² s⁻¹);研究弱光胁迫则相反。
一般性建议:如果没有特定目的,将光化光强度设置为植物生长光强的同等水平是一个安全且合理的起点。
二、光化光强度过高或过低对测试结果的影响
光化光强度直接驱动光合电子传递链,其设置不当会直接导致对植物生理状态的误判。
光化光强度过高的影响:
1、引发强烈光抑制(Photoinhibition):当光能输入远超过光合作用所能利用和耗散的能力时,会导致反应中心,特别是PSII的损伤。这会表现为最大光化学效率(Fv/Fm)的显著下降。
结果:你测量到的可能不是植物在“正常”状态下的性能,而是其在“胁迫”状态下的响应。这可能会夸大胁迫效应或掩盖其他处理的真实效果。
2、非光化学淬灭(NPQ)显著升高:植物为自我保护,会启动热耗散机制(NPQ)来散失过量光能。高光下NPQ会急剧增加。
结果:这本身是正常生理响应,但如果你关注的是光化学效率本身,过高的NPQ会使光化学淬灭(qP)和实际光化学效率(Y(II))降低,使得数据解读复杂化。
3、可能饱和甚至光破坏:
在极高光下,光合速率达到饱和且不再增加,而光损伤风险急剧增大。这会导致基于荧光参数计算的电子传递速率(ETR)与实际光合速率的关系偏离线性区域,ETR会高估实际碳同化能力。
4、样品灼伤:
物理上可能导致叶片或组织被灼伤,产生黄化斑点,影响测量区域的准确性。
光化光强度过低的影响:
1、光合机构未被充分激活:
光化光不足以为碳同化( Calvin循环)提供足够的ATP和NADPH,导致光合电子传递链“空转”,状态转换而非能量淬灭成为主要调节方式。
结果:光化学效率(Y(II))可能看起来很高,但这是一种“虚假的繁荣”,因为光合作用并没有全力运行。这可能会掩盖光合能力不足的问题。
2、无法诱导出足够的NPQ:
在弱光下,植物没有耗散热量的需求,NPQ水平很低。
结果:你无法准确评估植物的光保护能力。如果一个植物的NPQ诱导能力很弱,在弱光下你根本发现不了这个缺陷。
3、信噪比降低:
荧光信号较弱,可能导致测量的参数(如qP, Y(II))波动较大,重复性和准确性下降。
4、无法反映真实环境:
对于阳生植物,在远低于其生长光强的条件下测量,得到的是一种“低光适应”状态下的生理参数,无法代表其真实性能。
总结与建议
| 光化光强度 | 主要影响 | 可能导致的结果 |
|---|---|---|
| 过高 | 引发光抑制、NPQ极高、反应中心关闭或损伤 | 低估植物的潜在光合能力,测得的是胁迫状态 |
| 适宜 | 真实反映植物在当前环境下的光合运行状态和光保护能力 | 数据准确可靠,能代表植物的实际生理状态 |
| 过低 | 光合机构未充分激活、NPQ无法诱导、信噪比差 | 高估光化学效率,无法评估植物的耐光胁迫能力 |
最佳实践建议:
预实验是关键:在正式实验前,对少量样品进行光强梯度测试,观察关键参数(如Y(II), NPQ)的变化,找到能区分不同处理又不会造成严重光抑制的“最佳窗口”。
参考文献查阅同类研究中对类似材料通常使用什么光强。
明确实验目的:问自己“我想测量的是什么?”——是最大光合潜力、日常状态下的效率,还是胁迫响应?根据答案来设置光强。
记录并报告:在论文或报告中务必明确说明你所使用的光化光强度,这是保证实验可重复性的重要信息。
