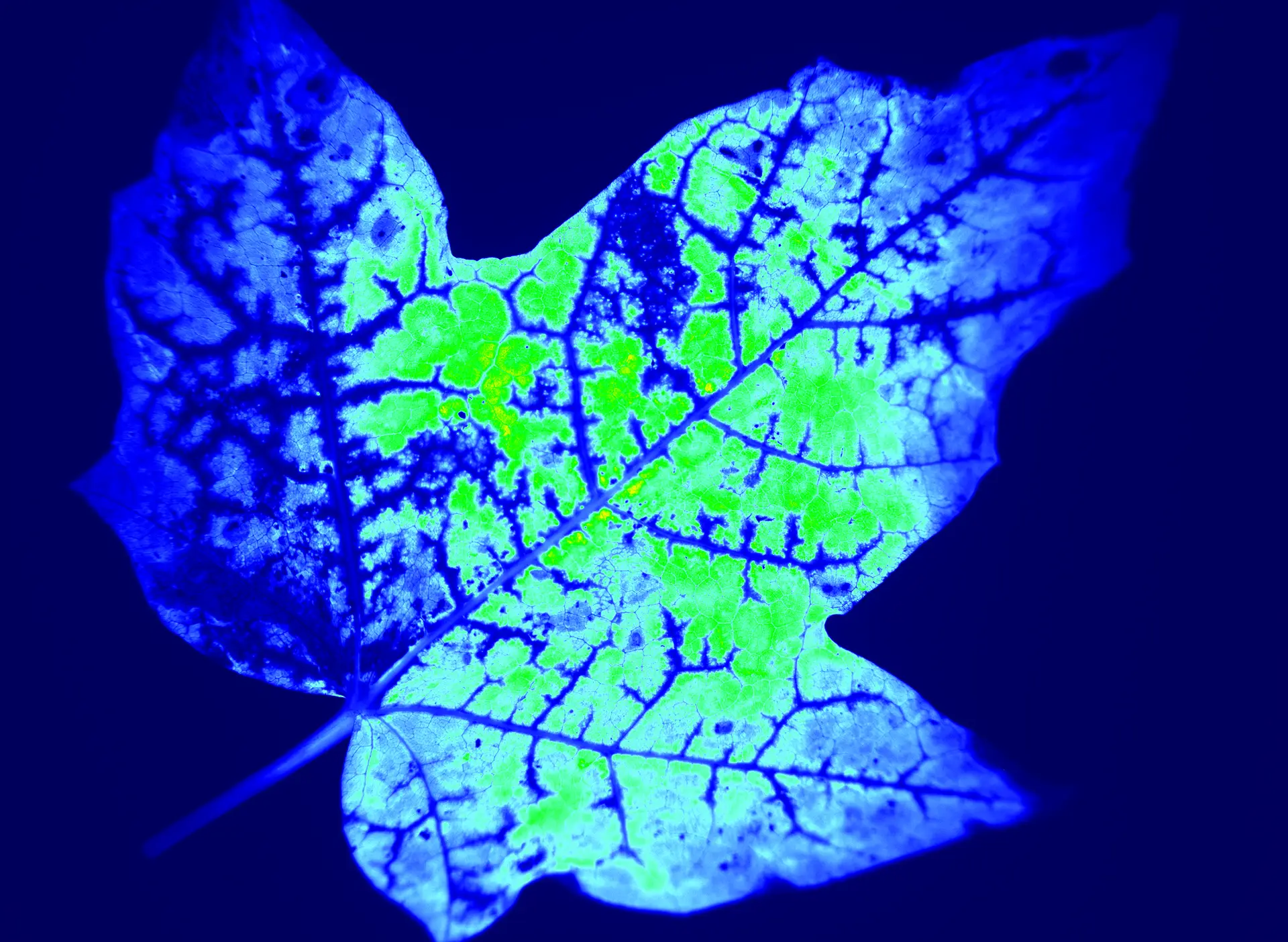
核心原则:一致性、标准化与稳定性
无论进行何种实验,都必须保证所有样品在处理和测量过程中的条件高度一致。
一、 样品准备与暗适应
这是最关键且最容易出错的步骤,直接决定了Fv/Fm初始值的准确性。
1、充分暗适应:
- 目的:让所有PSII反应中心完全“开放”,使电子传递链回到初始状态。这是准确测量Fm和Fo的基础。
- 时间:通常需要至少20-30分钟。对于胁迫下的植物、厚叶片或某些物种,可能需要更长时间(如45分钟)。
- 方法:使用专用的、不透光的暗适应夹或暗适应袋。普通文件夹或纱布袋可能会漏光。确保样品被完全覆盖,叶柄等部分也要遮光。将暗适应中的样品放置在稳定的生长环境中(如温度稳定的房间),避免放在冷、热或通风处。
2、样品状态一致性:
- 选择叶龄、大小和健康状况一致的叶片进行实验。
- 确保测量区域清洁,无灰尘、水珠或伤痕,这些都会干扰荧光信号。
二、 测量环境控制
环境条件会显著影响光合作用,从而影响荧光信号。
1、光照环境:
- 测量时,操作环境应保持微弱、稳定的光源,最好使用绿光或不激活光合作用的安全光,以免在测量前打断暗适应。
- 避免阳光直射或其他强光源直接照射样品和仪器镜头。
2、温度控制:
- 温度会影响酶的活性和膜流动性。尽量在恒温条件下进行测量。
- 如果进行温度胁迫实验,需使用温控平台确保样品温度精确。
3、稳定性:
- 将仪器和样品放置在稳固的实验台上,避免振动,以免成像模糊。
三、 仪器操作与参数设置
1、预热与校准:
- 按照制造商要求,提前打开仪器和电脑进行预热(通常需要15-30分钟),使光源和探测器性能稳定。
- 定期进行暗校准和平场校准。暗校准用于消除相机本身的噪音,平场校准用于消除镜头边缘的暗影和光照不均,这对于成像的定量分析至关重要。
2、参数设置优化:
- 饱和脉冲强度(SP):这是获取Fm的关键。强度必须足够高,以确保能关闭所有PSII反应中心。
- 检查方法:对一个样品逐步增加饱和脉冲强度,观察Fm值是否不再增加。如果Fm值随强度增加而升高,说明当前设置强度不足。应设置为能使Fm达到平台值的最低强度+10-20%的余量。过高的强度可能损伤样品。
- 测量光(ML)强度:用于测量Fo和稳态荧光(Fs)。强度必须足够低,以不引起任何光合作用。
- 增益(Gain):调节相机探测器的灵敏度。设置原则是:在测量Fm时,信号强度达到相机量程的70%-90%,但不能饱和(即像素值不能达到最大值)。信号太弱信噪比差,信号饱和则数据无效。
- 图像对焦与距离:确保相机镜头与样品表面平行,并根据说明书保持合适的工作距离,以获得清晰、不变形的图像。
四、 测量流程标准化
1、快速测量:
- 从暗适应夹中取出样品后,立即将其放置在测量平台上并进行测量。整个过程应在几秒钟内完成,任何延迟都会导致叶片开始进行光合作用,使Fm值下降,Fv/Fm被低估。
- 建议先对好焦、设置好程序,再放上样品。
2、测量顺序:
- 如果样品数量多,确保所有样品的暗适应时间相同。可以按固定时间间隔(如每30秒一个)进行测量,以保持处理一致性。
3、避免阴影:
- 操作者或仪器本身不要在样品上投下阴影。
五、 数据分析与质控
1、检查原始图像:
- 在分析前,务必先看一眼原始荧光图像(尤其是Fm图像)。
- 是否存在饱和区域?(图像中出现纯白色亮点)如果有,需要降低增益重新测量。
- 图像是否清晰? 对焦不准会导致数值平均化,降低空间分辨率。
- 是否有异物或损伤? 在分析时,应将这些区域排除(使用ROI工具)。
2、设置合理的阈值:
- 在分析软件中,设置Fo或Fm的阈值,以自动排除背景(无样品区域)和非叶片区域。这能保证统计分析只基于有效的叶片像素。
3、关注对照样品:
- 每次实验都包含已知健康的对照样品。如果对照样品的Fv/Fm值显著低于预期(如0.8),那么整个实验的测量条件可能存在问题。
- 总结清单:
暗适应充分(>30min)且完全避光 - 样品状态一致且清洁
- 环境稳定(光、温)
- 仪器已预热和校准
- 饱和脉冲强度经过优化验证
- 相机增益设置合理(无饱和)
- 测量过程快速(秒级)
- 分析前检查图像质量并排除无效区域
遵循以上要点,您将能最大限度地减少人为和技术误差,获得可靠、可重复的叶绿素荧光成像数据,从而对植物的光合生理状态做出准确的判断。
